Temperatur, Perpindahan Kalor, Pemuaian Zat : Pengertian, Pengukuran, Dan Perubahan
Temperatur, Perpindahan Kalor, Pemuaian Zat : Pengertian, Pengukuran, dan Perubahan - Pada penggalan ini, Anda akan diajak untuk sanggup menerapkan konsep kalor dan prinsip konservasi energi pada aneka macam perubahan energi dengan cara menganalisis efek kalor terhadap suatu zat, cara perpindahan kalor, serta sanggup menerapkan Asas Black dalam pemecahan masalah. Anda akan mencicipi panas kalau berada bersahabat dengan api yang menyala. Begitu pula kalau Anda memanaskan sebuah logam pada api yang menyala, Anda akan mencicipi logam tersebut menjadi panas dan mungkin Anda tidak sanggup memegangnya. Mengapa sanggup terjadi perpindahan panas, sedangkan Anda tidak menyentuh sumber panasnya tersebut? Kejadian ini sanggup juga disebut sebagai perpindahan kalor yang mempunyai arti sanggup menghantarkan dan menyerap energi. Perubahan wujud zat sering terjadi pada kehidupan sehari-hari dan mungkin sering Anda jumpai. Ketika sebuah es dipanaskan, es tersebut akan berubah wujudnya menjadi air. Begitu pula kalau air didinginkan pada sebuah lemari es, air tersebut akan berubah wujudnya menjadi es. Tahukah Anda, mengapa sanggup terjadi perubahan wujud menyerupai itu? Untuk lebih memahami materi mengenai zat dan kalor serta perpindahannya, pelajari bahasan-bahasan berikut ini dengan baik.
A. Pengertian Temperatur
Sangatlah sulit untuk menawarkan definisi temperatur menurut konsep yang umum digunakan, menyerupai pada besaran lain. Namun demikian, Anda sanggup memakai adanya kesepadanan (equality) perubahan temperatur terhadap perubahan sifat lain dari suatu benda. Temperatur sanggup didefinisikan sebagai sifat fisik suatu benda untuk memilih apakah keduanya berada dalam kesetimbangan termal. Dua buah benda akan berada dalam kesetimbangan termal kalau keduanya mempunyai temperatur yang sama.
1. Pengukuran Temperatur
Apabila dua benda berada dalam kesetimbangan termal dengan benda ketiga maka keduanya berada dalam kesetimbangan termal. Pernyataan menyerupai ini dikenal sebagai aturan ke nol termodinamika, yang sering mendasari pengukuran temperatur. Materi mengenai termodinamika akan Anda pelajari lebih mendalam di Kelas XI. Berdasarkan prinsip ini, kalau Anda ingin mengetahui apakah dua benda mempunyai temperatur yang sama maka kedua benda tersebut tidak perlu disentuh dan diamati perubahan sifatnya terhadap waktu, yang perlu dilakukan ialah mengamati apakah kedua benda tersebut, masing-masing berada dalam kesetimbangan termal dengan benda ketiga? Benda ketiga tersebut ialah termometer.
Benda apapun yang mempunyai sedikitnya satu sifat yang berubah terhadap perubahan temperatur sanggup dipakai sebagai termometer. Sifat semacam ini disebut sebagai sifat termometrik (thermometric property). Senyawa yang mempunyai sifat termometrik disebut senyawa termometrik. Temperatur zat yang diukur sama besarnya dengan skala yang ditunjukkan oleh termometer ketika terjadi kesetimbangan termal antara zat dengan termometer. Jadi, temperatur yang ditunjukkan oleh termometer sama dengan temperatur zat yang diukur.
Zat cair yang umum dipakai dalam termometer ialah air raksa. Hal ini dikarenakan air raksa mempunyai keunggulan dibandingkan zat cair lainnya. Keunggulan air raksa dari zat cair lainnya, yaitu
- dapat menyerap panas suatu benda yang akan diukur sehingga temperatur air raksa sama dengan temperatur benda yang diukur,
- dapat dipakai untuk mengukur temperatur yang rendah hingga temperatur yang lebih tinggi lantaran air raksa mempunyai titik beku pada temperatur –39 °C dan titik didihnya pada temperatur 357 °C,
- tidak membasahi dinding tabung sehingga pengukurannya menjadi lebih teliti,
- pemuaian air raksa teratur atau linear terhadap kenaikan temperatur, kecuali pada temperatur yang sangat tinggi, dan
- mudah dilihat lantaran air raksa sanggup memantulkan cahaya.
Selain air raksa, sanggup juga dipakai alkohol untuk mengisi tabung termometer. Akan tetapi, alkohol tidak sanggup mengukur temperatur yang tinggi lantaran titik didihnya 78 °C, namun alkohol sanggup mengukur temperatur yang lebih rendah lantaran titik bekunya pada temperatur –144 °C. Jadi, termometer yang berisi alkohol baik untuk mengukur temperatur yang rendah, tetapi tidak sanggup mengukur temperatur yang lebih tinggi.
2. Skala pada Beberapa Termometer
Ketika mengukur temperatur dengan memakai termometer, terdapat beberapa skala yang digunakan, di antaranya skala Celsius, skala Reamur, skala Fahrenheit, dan skala Kelvin. Keempat skala tersebut mempunyai perbedaan dalam pengukuran suhunya. Berikut rentang temperatur yang dimiliki setiap skala.
a. Termometer skala Celsius
Memiliki titik didih air 100 °C dan titik bekunya 0 °C. Rentang temperaturnya berada pada temperatur 0 °C – 100 °C dan dibagi dalam 100 skala.
b. Temometer skala Reamur
Memiliki titik didih air 80 °R dan titik bekunya 0 °R. Rentang temperaturnya berada pada temperatur 0 °R – 80 °R dan dibagi dalam 80 skala.
c. Termometer skala Fahrenheit
Memiliki titik didih air 212 °F dan titik bekunya 32 °F. Rentang temperaturnya berada pada temperatur 32 °F – 212 °F dan dibagi dalam 180 skala.
d. Termometer skala Kelvin
Memiliki titik didih air 373,15 K dan titik bekunya 273,15 K. Rentang temperaturnya berada pada temperatur 273,15 K – 373,15 K dan dibagi dalam 100 skala. Jadi, kalau diperhatikan pembagian skala tersebut, satu skala dalam derajat Celsius sama dengan satu skala dalam derajat Kelvin, sementara satu skala Celsius kurang dari satu skala Reamur dan satu skala Celsius lebih dari satu skala Fahrenheit. Secara matematis perbandingan keempat skala tersebut, yaitu sebagai berikut.
Mengukur Temperatur
Temperatur zat apapun eksklusif berkaitan dengan ratarata energi gerak atom atau molekul pembentuknya. Walaupun temperatur terendah pada termometer ini (0 – 2) °C atau (0 – 4) °F, temperatur yang terendah yang sanggup dicapai lebih kurang (0 – 273)°C atau –459 °F yang disebut temperatur nol mutlak. Temperatur ini hanya sanggup dijumpai apabila atom dan molekul tidak lagi mengandung energi gerak sama sekali. Celsius (C) dan Fahrenheit (F) ialah dua skala temperatur yang paling lazim digunakan. (Sumber: Jendela Iptek, 1997)
Contoh Soal 1 :
Misalkan Ucok menciptakan sebuah termometer yang disebut dengan termometer X. Pada termometer ini air membeku pada 0 °X dan air mendidih pada 150 °X. Bagaimanakah kekerabatan termometer ini dengan termometer dalam skala Celsius?
Kunci Jawaban :
Pada termometer X, rentang temperatur yang dimilikinya, yakni dari 0 °X – 150 °X sehingga skala pada termometer ini dibagi dalam 150 skala. Perbandingan antara termometer X dan termometer Celsius, yakni :
Jadi, kekerabatan antara termometer ini dengan termometer Celsius ialah t °C = 2/3 t °X.
B. Pemuaian Zat
Anda mungkin pernah melihat sambungan rel kereta api dibentuk renggang atau bingkai beling lebih besar daripada kacanya. Hal ini dibentuk untuk menghindari jawaban dari terjadinya pemuaian. Pemuaian terjadi kalau benda yang sanggup memuai diberi panas. Ada 3 jenis pemuaian jenis zat, yaitu pemuaian zat padat, pemuaian zat cair, dan pemuaian zat gas. Pada penggalan ini hanya akan dibahas pemuaian zat padat.
1. Pemuaian Panjang
Jika temperatur dari sebuah benda naik, kemungkinan besar benda tersebut akan mengalami pemuaian. Misalnya, sebuah benda yang mempunyai panjang L0 pada temperatur T akan mengalami pemuaian panjang sebesar ΔL kalau temperatur dinaikan sebesar ΔT. Secara matematis, perumusan pemuaian panjang sanggup dituliskan sebagai berikut.
ΔL = α L0ΔT (1-1)
dengan α ialah koefisien muai panjang.
Satuan dari α ialah kebalikan dari satuan temperatur skala Celsius (1/°C) atau kelvin (1/K). Tabel berikut ini memperlihatkan nilai dari koefisien muai panjang untuk aneka macam zat.
Bahan | Α (1/K) |
Aluminium | 24 × 10–6 |
Kuningan | 19 × 10–6 |
Karbon | |
· Intan | 1,2 × 10–6 |
· Grafit | 7,9 × 10–6 |
Tembaga | 17 × 10–6 |
Gelas | |
· Biasa | 9 × 10–6 |
· Pyrex | 3,2 × 10–6 |
Es | 51 × 10–6 |
Invar | 1 × 10–6 |
Baja | 11 × 10–6 |
Sumber: Physics, 1995 | |
Contoh Soal 2 :
Sebuah kuningan mempunyai panjang 1 m. Tentukanlah pertambahan panjang kuningan tersebut kalau temperaturnya naik dari 10 °C hingga 40 °C.
Kunci Jawaban :
Diketahui: L0 = 1 m,
ΔT = 40 °C – 10 °C = 30 °C = 303,15 K, dan
α kuningan = 19 × 10–6/K.
ΔL = α L0 ΔT
ΔL = (19 × 10–6/K) (1 m) (303,15 K)
ΔL = 5,76 × 10–3 = 5,76 mm
Jadi, pertambahan panjang kuningan sehabis temperaturnya naik menjadi 40° ialah 5,76 mm.
2. Pemuaian Luas
Sebuah benda yang padat, baik bentuk persegi maupun silinder, niscaya mempunyai luas dan volume. Seperti halnya pada pemuaian panjang, ketika benda dipanaskan, selain terjadi pemuaian panjang juga akan mengalami pemuaian luas. Perumusan pada pemuaian luas hampir sama menyerupai pada pemuaian panjang, yaitu sebagai berikut :
ΔA = βΔ0AT (1-3)
dengan β ialah koefisien muai luas.
satuan dari β ialah /K sama menyerupai koefisien muai panjang (α).
 |
| Gambar 2. Logam berbentuk persegi kalau dipanaskan akan memuai. |
Coba Anda perhatikan sebuah tembaga berbentuk persegi sama sisi. Misalkan, panjang sisi tembaga adalah L0 maka luas tembaga adalah L02. Jika tembaga tersebut dipanasi hingga terjadi perubahan temperatur sebesar ΔT maka sisi-sisi tembaga akan memuai dan panjang sisi tembaga menjadi L0 + ΔT. Luas tembaga sehabis memuai akan berubah menjadi (L0 + ΔT)2 dan perubahan luas sehabis pemuaian ialah :
ΔA = (L0 + ΔL)2 – L02
ΔA = L02 + 2L0ΔL + ΔL2 – L02
ΔA = 2L0ΔL + ΔL2
dari perumusan koefisien muai luas, yaitu :
Oleh lantaran perubahan panjang ΔL tembaga sangatlah kecil maka nilai ΔL2 dapat diabaikan. Jika ditulis ulang, persamaan tersebut menjadi :
menyerupai yang telah Anda ketahui bahwa :
maka,
β = 2α (1-5)
Contoh Soal 3 :
Sebuah batang aluminium mempunyai luas 100 cm2. Jika batang aluminium tersebut dipanaskan mulai dari 0 °C hingga 30 °C, berapakah perubahan luasnya sehabis terjadi pemuaian? (Diketahui: α = 24 × 10–6/K).
Kunci Jawaban :
Diketahui:
A0 = 100 cm2 = 1 m2,
ΔT = 30 °C – 0 °C = 30 °C = 303,15 K, dan
β = 2α = 48 × 10–6/K.
ΔA = β A0ΔT
ΔA = 48 × 10–6/K × 1 m2 × 303,15 K
ΔA = 0,0145 m2
Jadi, perubahan luas bidang aluminium sehabis pemuaian ialah 0,0145 m2.
3. Pemuaian Volume
Seperti yang telah dibahas sebelumnya, setiap benda yang padat niscaya mempunyai volume. Jika panjang sebuah benda sanggup memuai ketika dipanaskan maka volume benda tersebut juga ikut memuai. Perumusan untuk pemuaian volume sama dengan perumusan panjang dan luas, yaitu :
dengan γ ialah koefisien muai volume .
Perlu Anda ketahui terdapat kekerabatan antara α dan β terhadap waktu γ, yaitu :
γ = 3α
γ = 3/2 β (1-8)
Contoh Soal 4 :
Sebuah bola yang mempunyai volume 50 m3 jika dipanaskan hingga mencapai temperatur 50 °C. Jika pada kondisi awal kondisi tersebut mempunyai temperatur 0 °C, tentukanlah volume simpulan bola tersebut sehabis terjadi pemuaian (Diketahui α = 17 × 10–6/K)
Kunci Jawaban :
Diketahui :
V0 = 50 m3,
ΔT = 50°C – 0°C = 50°C = 323,15 K, dan
γ = 3α = 51 × 10–6/K.
ΔV = γVoΔT
ΔV = 51 × 10–6/K × 50 m3 × 323,15 K
ΔV = 0,82 m3
ΔV = V – Vo
V = ΔV + Vo
V = 0,82 m3 + 50 m3 = 50,82 m3
Jadi, volume simpulan bola sehabis pemuaian ialah 50,82 m3.
Percobaan Fisika Sederhana 1 :
Sediakanlah sebuah gelas beling dan sebuah gelas plastik atau gelas keramik (mug). Masukkan air mendidih (100 °C) kepada kedua gelas tersebut. Amatilah apa yang terjadi. Mengapa gelas beling pecah, sedangkan gelas plastik atau gelas keramik tidak pecah? Apakah ada hubungannya dengan konsep pemuaian? Coba Anda jelaskan dengan memakai bahasa Anda sendiri. Jika perlu, diskusikan bersama sobat atau guru Anda dan presentasikan kesannya di depan kelas.
C. Pengertian Kalor
Misalkan, dua buah zat yang mempunyai temperatur berbeda dicampurkan pada sebuah wadah. Maka temperatur kedua benda tersebut akan menjadi sama. Besarnya temperatur simpulan berada di antara temperatur awal kedua zat tersebut. Pada tanda-tanda ini, kalor berpindah dari temperatur tinggi ke temperatur yang lebih rendah hingga mencapai temperatur setimbangnya. Pada 1850, untuk pertama kalinya Joule memakai sebuah alat yang di dalamnya terdapat beban-beban yang jatuh dan merotasikan sekumpulan pengaduk di dalam sebuah wadah air yang tertutup. Dalam satu siklus, beban-beban yang jatuh tersebut melaksanakan sejumlah kerja pada air tersebut dengan massa air ialah m dan air tersebut mengalami kenaikan temperatur sebesar Δt. Percobaan ini mengambarkan ihwal adanya energi yang menyebabkan timbulnya kalor dalam siklus tersebut.
Kalor sanggup didefinisikan sebagai proses transfer energi dari suatu zat ke zat lainnya dengan diikuti perubahan temperatur. Satuan kalor ialah joule (J) yang diambil dari nama seorang ilmuwan yang telah berjasa dalam bidang ilmu Fisika, yaitu James Joule. Satuan kalor lainnya ialah kalori. Hubungan satuan joule dan kalori, yakni 1 kalori = 4,184 joule.
1. Kalor Jenis dan Kapasitas Kalor
Apabila temperatur dari suatu benda dinaikkan dengan besar kenaikan temperatur yang sama, ternyata setiap benda akan menyerap energi kalor dengan besar yang berbeda. Misalnya, terdapat empat buah bola masing-masing terbuat dari aliminium, besi, kuningan, dan timah. Keempat bola ini mempunyai massa sama dan ditempatkan di dalam suatu daerah yang berisi air mendidih. Setelah 30 menit, keempat bola akan mencapai kesetimbangan termal dengan air dan akan mempunyai temperatur yang sama dengan temperatur air. Kemudian, keempat bola diangkat dan ditempatkan di atas kepingan parafin. Bola aluminium sanggup melelehkan parafin dan jatuh menembus parafin. Beberapa sekon kemudian, bola besi mengalami bencana yang sama. Bola kuningan hanya sanggup melelehkan parafin sebagian, sedangkan bola timah hampir tidak sanggup melelehkan parafin.
Bagaimanakah Anda sanggup menjelaskan bencana yang terjadi pada keempat bola tersebut? Keempat bola tersebut menyerap kalor dari air mendidih, kemudian memindahkan kalor tersebut pada parafin sehingga parafin meleleh. Oleh lantaran setiap benda mempunyai kemampuan berbeda untuk melelehkan parafin, setiap bola akan memindahkan kalor dari air ke parafin dengan besar yang berbeda. Kemampuan yang dimiliki setiap benda ini bekerjasama dengan kalor jenis benda tersebut. Kalor jenis suatu benda sanggup didefinisikan sebagai jumlah kalor yang diharapkan untuk menaikkan temperatur 1 kg suatu zat sebesar 1K. Kalor jenis memperlihatkan kemampuan suatu benda untuk menyerap kalor. Semakin besar kalor jenis suatu benda, semakin besar pula kemampuan benda tersebut untuk menyerap kalor. Secara matematis, kalor jenis suatu zat sanggup dituliskan sebagai berikut.
dengan:
c = kalor jenis suatu zat (J/kg K),
Q = kalor (J),
m = massa benda (kg), dan
ΔT = perubahan temperatur (K).
Untuk suatu benda, faktor mc dipandang sebagai satu kesatuan dan faktor ini disebut sebagai kapasitas kalor. Secara matematis dituliskan sebagai berikut.
Satuan kapasitas kalor ialah J/K. Jika Persamaan (1–9) dan Persamaan (1–10) diuraikan, besarnya kalor suatu zat ialah :
Q = m cΔT (1-11)
Q = C ΔT (1-12)
Contoh Soal 5 :
Energi kalor yang diharapkan untuk memanaskan air dari 30 °C hingga dengan 80 °C dengan massa air 500 gram (cair = 4.200 J/kgK) ialah ....
a. 350.000 joule
b. 378.000 joule
c. 252.000 joule
d. 152.000 joule
e. 105.000 joule
Kunci Jawaban :
Diketahui:
m = 500
g = 0,5 kg,
g = 0,5 kg,
c = 4.200 J/kgK, dan
ΔT = (80–30) °C = 50 °C.
Q = mc ΔT
Q = (0,5 kg) × (4.200 J/kgK) × (50 °C)
Q = 105.000 joule
Jawab : e
Contoh Soal 6 :
Air sebanyak 100 gram yang mempunyai temperatur 25 °C dipanaskan dengan energi sebesar 1.000 kalori. Jika kalor jenis air 1 kal/g oC, tentukanlah temperatur air sehabis pemanasan tersebut.
Kunci Jawaban :
Diketahui:
m = 100 gram,
m = 100 gram,
T0 = 25 °C,
cair = 1 kal/g °C, dan
Q = 1.000 kal.
Dengan memakai Persamaan (1–11), diperoleh :
Q = mc ΔT
ΔT = Q / mc = (1.000 kal) / (100 gram × 1 kal/g °C)
ΔT = 10°C
Perubahan temperatur mempunyai arti selisih antara temperatur simpulan air sehabis pemanasan terhadap temperatur awal, atau secara matematis dituliskan sebagai berikut.
ΔT = T – T0
10 °C = T – 25 °C
T = 35 °C
Jadi, temperatur simpulan air sehabis pemanasan ialah 35 °C.
2. Perubahan Wujud Zat
Setiap zat mempunyai kecenderungan untuk berubah kalau zat tersebut diberikan temperatur yang tinggi (dipanaskan) ataupun temperatur yang rendah (didinginkan). Kecenderungan untuk berubah wujud ini disebabkan oleh kalor yang dimiliki setiap zat. Suatu zat sanggup berkembang menjadi tiga wujud zat, di antaranya cair, padat, dan gas. Perubahan wujud zat ini diikuti dengan perembesan dan pelepasan kalor.
a. Kalor Penguapan dan Pengembunan
Kalor penguapan ialah kalor yang dibutuhkan oleh suatu zat untuk menguapkan zat tersebut. Jadi, setiap zat yang akan menguap membutuhkan kalor. Adapun kalor pengembunan ialah kalor yang dilepaskan oleh uap air yang berubah wujud menjadi air. Jadi, pada setiap pengembunan akan terjadi pelepasan kalor. Besarnya kalor yang dibutuhkan pada ketika penguapan dan kalor yang dilepaskan pada ketika pengembunan ialah sama. Secara matematis, kalor penguapan dan pengembunan sanggup dituliskan sebagai berikut.
Q = m L (1-13)
dengan :
Q = kalor yang dibutuhkan ketika penguapan atau kalor yang dilepaskan ketika pengembunan,
m = massa zat, dan
L = kalor laten penguapan atau pengembunan.
b. Kalor Peleburan dan Pembekuan
Pernahkah Anda mendengar atau mendapatkan isu ihwal bencana mencairnya gunung-gunung es di kutub utara jawaban pemanasan global? Mencair atau meleburnya es di kutub utara disebabkan oleh adanya pemanasan. Jika benda mengalami peleburan, perubahan wujud yang terjadi ialah dari wujud zat padat menjadi zat cair. Dalam hal ini, akan terjadi perembesan kalor pada benda. Adapun perubahan wujud zat dari cair ke padat disebut sebagai proses pembekuan. Dalam hal ini, akan terjadi proses pelepasan kalor. Besarnya kalor yang dibutuhkan pada ketika peleburan dan besarnya kalor yang dilepaskan dalam proses pembekuan ialah sama. Perumusan untuk kalor peleburan dan pembekuan sama dengan perumusan pada kalor penguapan dan pengembunan, yakni sebagai berikut.
Q = m L (1–14)
dengan :
Q = kalor yang dibutuhkan ketika peleburan atau kalor yang dilepaskan ketika pembekuan,
m = massa zat, dan
L = kalor laten peleburan atau pembekuan.
Contoh Soal 7 :
Berapakah besarnya kalor yang dibutuhkan untuk mencairkan es sebanyak 500 gram pada temperatur 0 °C menjadi cair seluruhnya yang mempunyai temperatur 10 °C Diketahui kalor laten peleburan es menjadi air sebesar 80 kal/g.
Kunci Jawaban :
Diketahui:
L = 80 kal/g, dan
L = 80 kal/g, dan
m = 500 gram.
Dengan memakai Persamaan (1–14), diperoleh
Q = m L
Q = 500 gram × 80 kal/g
Q = 40.000 kal
Q = 40 kkal
Jadi, besarnya kalor yang dibutuhkan untuk meleburkan es menjadi cair seluruhnya ialah sebesar 40 kkal.
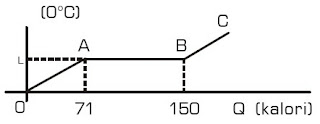
Contoh Soal 8 :
Grafik berikut ini menyatakan kekerabatan antara temperatur (t) dengan kalor (Q) yang diberikan pada 1 gram zat padat.
Besar kalor lebur zat padat tersebut ialah ....
a. 71 kalori/g
b. 79 kalori/g
c. 80 kalori/g
d. 811 kalori/g
e. 150 kalori/g
Kunci Jawaban :
Diketahui:
mzat = 1 gram.
Zat padat tersebut mengalami peleburan pada temperatur 1 (grafik AB). Pada kurva AB.
ΔQ = 150 – 71 = 79 kal.
Dengan demikian, kalor lebur zat padat sanggup dihitung sebagai berikut :
ΔT = mQ
Q = ΔT / m = 79 / 1 = 79 kal/gram
3. Hubungan Kalor Laten dan Perubahan Wujud
Sebuah benda sanggup berubah wujud ketika diberi kalor. Coba Anda perhatikan sikap suatu benda ketika dipanaskan. Apabila suatu zat padat, contohnya es dipanaskan, es tersebut akan menyerap kalor dan beberapa usang kemudian berubah wujud menjadi zat cair. Perubahan wujud zat dari padat menjadi cair ini disebut proses melebur. Temperatur pada ketika zat mengalami peleburan disebut titik lebur zat. Adapun proses perubahan wujud zat dari cair menjadi padat disebut sebagai proses pembekuan dan temperatur ketika zat mengalami proses pembekuan disebut titik beku zat.
Jika zat cair dipanaskan akan menguap dan berubah wujud menjadi gas. Perubahan wujud dari zat cair menjadi uap (gas) disebut menguap. Pada bencana penguapan dibutuhkan kalor. Proses penguapan sanggup terjadi dalam kehidupan sehari-hari, contohnya Anda mencelupkan tangan Anda ke dalam cairan spiritus atau alkohol. Spiritus atau alkohol ialah zat cair yang gampang menguap. Untuk melaksanakan penguapan ini, spiritus atau alkohol menyerap panas dari tangan Anda sehingga tangan Anda terasa dingin. Peristiwa lain yang memperlihatkan bahwa proses penguapan membutuhkan kalor ialah pada air yang mendidih. Penguapan hanya terjadi pada permukaan zat cair dan sanggup terjadi pada sembarang temperatur, sedangkan mendidih hanya terjadi pada seluruh penggalan zat cair dan hanya terjadi pada temperatur tertentu yang disebut dengan titik didih. Proses kebalikan dari menguap ialah mengembun, yakni perubahan wujud dari uap menjadi cair.
Ketika sedang berubah wujud, baik melebur, membeku, menguap, dan mengembun, temperatur zat akan tetap, walaupun terdapat pelepasan atau perembesan kalor. Dengan demikian, terdapat sejumlah kalor yang dilepaskan atau diserap pada ketika perubahan wujud zat, tetapi tidak dipakai untuk menaikkan atau menurunkan temperatur. Kalor ini disebut sebagai kalor laten dan disimbolkan dengan karakter L. Besarnya kalor ini bergantung pada jumlah zat yang mengalami perubahan wujud (massa benda). Jadi, kalor laten ialah kalor yang dibutuhkan oleh suatu benda untuk mengubah wujudnya per satuan massa.
Mengapa kalor yang diserap oleh suatu zat padat ketika melebur atau menguap tidak sanggup menaikkan temperaturnya? Berdasarkan teori kinetik, pada ketika melebur atau menguap, kecepatan getaran molekul bernilai maksimum. Kalor yang diserap tidak menambah kecepatannya, tetapi dipakai untuk melawan gaya ikat antarmolekul zat tersebut.
Ketika molekul-molekul ini melepaskan diri dari ikatannya, zat padat berkembang menjadi zat cair atau zat cair berkembang menjadi gas. Setelah seluruh zat padat melebur atau menguap, temperatur zat akan bertambah kembali. Peristiwa kebalikannya terjadi juga pada ketika melebur, membeku, atau mengembun.
Kalor laten pembekuan besarnya sama dengan kalor laten peleburan yang disebut sebagai kalor lebur. Kalor lebur es L pada temperatur dan tekanan normal ialah 334 kJ/kg. Kalor laten penguapan besarnya sama dengan kalor laten pengembunan, yang disebut sebagai kalor uap. Kalor uap air L pada temperatur dan tekanan normal ialah 2.256 kJ/kg.
 |
| Gambar 3. Grafik perubahan temperatur dan berubahan wujud zat pada sebuah es. |
Perhatikan Gambar 3. yang memperlihatkan proses perubahan temperatur dan wujud zat pada sebuah es. Dari gambar tersebut terdapat proses perubahan temperatur dan wujud zat yang terjadi, yakni sebagai berikut.
a. Proses A – B merupakan proses kenaikan temperatur dari sebongkah es. Pada proses kenaikan temperatur ini, grafik yang terjadi ialah linear. Pada grafik AB, kalor dipakai untuk menaikkan temperatur.
QAB = mes ces ΔT
QAB = mes ces (0oC – (–T1))
QAB = mes ces T1
b. Proses B – C merupakan proses perubahan wujud zat dari es menjadi air. Pada grafik BC, kalor tidak dipakai untuk menaikkan atau menurunkan temperatur benda, tetapi hanya dipakai untuk mengubah wujud zat benda tersebut, yakni dari wujud es menjadi air.
QBC = mes L
c. Pada grafik C – D, terjadi proses kenaikan temperatur yang sama dengan proses pada (a). Akan tetapi, pada proses ini yang dinaikkan suhunya ialah air dari 0 °C sampai 100 °C.
QCD = mair cair ΔT
QCD = mair cair (100 °C – 0 °C)
QCD = mair cair 100 °C
d. Sama halnya pada proses B – C, proses D – E tidak mengalami perubahan temperatur, tetapi yang terjadi hanya perubahan wujud zat dari air menjadi uap.
QDE = mair L
Contoh Soal 9 :
Es yang massanya 125 gram dan mempunyai temperatur 0 °C, dimasukkan ke dalam 500 gram air yang mempunyai temperatur 20 °C. Ternyata, es melebur seluruhnya. Jika kalor lebur es = 80 kalori/gram °C, temperatur simpulan gabungan ialah ....
a. 0°C
b. 5°C
c. 10°C
d. 15°C
e. 20°C
Kunci Jawaban :
Jawab: a
Es yang massanya 125 gram dan mempunyai temperatur 0 °C, dimasukkan ke dalam 500 gram air yang mempunyai temperatur 20 °C. Ternyata, es melebur seluruhnya. Jika kalor lebur es = 80 kalori/gram °C, temperatur simpulan gabungan ialah ....
a. 0°C
b. 5°C
c. 10°C
d. 15°C
e. 20°C
Kunci Jawaban :
mair cair Δair = mcampuran ccampuran Δcampuran + mes
500 × 1 × (20 – takhir) = 625 × 1 × (takhir – 0) + 125 × 80
10.000 – 500 takhir = 625 takhir + 10.000
625 takhir + 500 takhir = 10.000 – 10.000
1.125 takhir = 0
takhir = 0 °CJawab: a
4. Asas Black
Kalor ialah energi yang dipindahkan dari benda yang mempunyai temperatur tinggi ke benda yang mempunyai temperatur lebih rendah sehingga pengukuran kalor selalu bekerjasama dengan perpindahan energi. Energi ialah awet sehingga benda yang mempunyai temperatur lebih tinggi akan melepaskan energi sebesar QL dan benda yang mempunyai temperatur lebih rendah akan mendapatkan energi sebesar QT dengan besar yang sama.
Secara matematis, pernyataan tersebut sanggup ditulis sebagai berikut.
QLepas = QTerima (1-15)
Persamaan (1–15) menyatakan aturan kekekalan energi pada pertukaran kalor yang disebut sebagai Asas Black. Nama aturan ini diambil dari nama seorang ilmuwan Inggris sebagai penghargaan atas jasa-jasanya, yakni Joseph Black (1728–1799). Pengukuran kalor sering dilakukan untuk memilih kalor jenis suatu zat. Jika kalor jenis suatu zat diketahui, kalor yang diserap atau dilepaskan sanggup ditentukan dengan mengukur perubahan temperatur zat tersebut. Kemudian, dengan memakai persamaan
Q = m c ΔT
besarnya kalor sanggup dihitung. Ketika memakai persamaan ini, perlu diingat bahwa temperatur naik berarti zat mendapatkan kalor, dan temperatur turun berarti zat melepaskan kalor.
 |
| Gambar 4. Kalorimeter sebagai alat ukur kalor. |
Kalorimeter ialah alat yang dipakai untuk mengukur kalor. Salah satu bentuk kalorimeter, tampak pada Gambar 4. Kalorimeter ini terdiri atas sebuah ember logam dengan kalor jenisnya telah diketahui. Bejana ini biasanya ditempatkan di dalam ember lain yang agak lebih besar. Kedua ember dipisahkan oleh materi penyekat, contohnya gabus atau wol. Kegunaan ember luar ialah sebagai pelindung semoga pertukaran kalor dengan lingkungan di sekitar kalorimeter sanggup dikurangi. Kalorimeter juga dilengkapi dengan batang pengaduk. Pada waktu zat dicampurkan di dalam kalorimeter, air di dalam kalorimeter perlu diaduk semoga diperoleh temperatur merata dari percampuran dua zat yang suhunya berbeda. Batang pengaduk ini biasanya terbuat dan materi yang sama menyerupai materi ember kalorimeter. Zat yang diketahui kalor jenisnya dipanaskan hingga temperatur tertentu. Kemudian, zat tersebut dimasukkan ke dalam kalorimeter yang berisi air dengan temperatur dan massanya yang telah diketahui. Selanjutnya, kalorimeter diaduk hingga suhunya tetap.
Tokoh Fisika :
Joseph Black mengira bahwa kapasitas panas merupakan jumlah panas yang sanggup ditampung oleh suatu benda. Hal ini bekerjsama merupakan ukuran ihwal jumlah tenaga yang diharapkan untuk menaikan temperatur suatu benda dalam jumlah tertentu. Misalnya, untuk menaikkan temperatur 1 kg (2,2 lb) air sebesar 1 °C (1,8 °F) dibutuhkan lebih banyak panas daripada menaikkan temperatur 1 kg besi dengan kenaikan temperatur yang sama. (Sumber: Jendela Iptek, 1997)
D. Perpindahan Kalor
Pada sebuah benda, perpindahan kalor atau perambatan kalor terjadi dari benda yang bersuhu tinggi ke benda yang bersuhu rendah. Kalor sanggup merambat dengan tiga cara, di antaranya secara konduksi (hantaran), secara konveksi (aliran), dan secara radiasi (pancaran). Berikut pembahasan mengenai setiap jenis perambatan kalor tersebut.
1. Perpindahan Kalor Secara Konduksi
Jika salah satu ujung batang logam dimasukkan ke dalam api atau dipanaskan, ujung batang yang lainnya akan ikut menjadi panas, walaupun tidak ikut dimasukkan ke dalam api. Mengapa demikian? Atom-atom di dalam zat padat yang dipanaskan tersebut akan bergetar dengan sangat kuat. Kemudian, atom-atom tersebut akan memindahkan sebagian energi yang dimilikinya ke atom-atom tetangga terdekat yang ditumbuknya. Atom tetangga ini menumbuk atom tetangga lainnya dan seterusnya sehingga terjadi hantaran energi di dalam zat padat tersebut. Untuk materi logam, terdapat elektron-elektron yang sanggup bergerak bebas yang juga ikut berperan dalam merambatkan energi tersebut. Perpindahan kalor yang tidak diikuti perpindahan massa ini disebut konduksi.
 |
| Gambar 5. Rambatan kalor di dalam konduktor. |
Kalor yang mengalir dalam batang per satuan waktu sanggup dinyatakan dalam hubungan:
dengan:
T1 = ujung batang logam bersuhu tinggi,
T1 = ujung batang logam bersuhu tinggi,
T2 = ujung batang logam bersuhu rendah,
A = luas penampang hantaran kalor dan batang logam,
L = panjang batang,
K = koefisien konduksi termal, dan
H = jumlah kalor yang merambat pada batang per satuan waktu per satuan luas.
Dalam kehidupan sehari-hari, teladan bencana konduksi ini sanggup Anda temukan ketika Anda memasak makanan. Panci yang dipakai untuk memasak akan mendapatkan panas atau kalor di setiap bagiannya, walaupun penggalan panci yang terkena api hanyalah di penggalan bawahnya. Perambatan kalor secara konduksi ini juga terjadi pada sendok yang digunakan. Oleh lantaran itu, tangkai sendok penggorengan dilapisi dengan materi yang tidak menghantarkan kalor, menyerupai plastik atau kayu. Berikut tabel yang menyatakan nilai konduktivitas termal beberapa zat.
Tabel 2. Konduktivitas Termal Beberapa Zat
Zat/Bahan | K (Kj / ms K) |
Logam: Perak Tembaga Aluminium Kuningan Besi/Baja Zat Padat Lainnya: Beton Kaca Batu bata Kayu cemara Zat cair: Air Bahan isolator: Serbuk gergaji Gabus Wol gelas Kapuk Gas: Hidrogen Udara | 4,2 × 10-1 3,8 × 10-1 2,1 × 10-1 1,0 × 10-2 4,6 × 10-3 1,7 × 10-3 8,0 × 10-4 7,1 × 10-4 1,2 × 10-4 5,7 × 10-4 5,9 × 10-5 4,0 × 10-5 3,9 × 10-5 3,5 × 10-5 1,7 × 10-4 2,3 × 10-5 |
Sumber: Physics, 1995 | |
Contoh Soal 9 :
Batang aluminium (KAl = 500 × 10–1 kal/m s °C) luas penampang ujungnya 1 cm2 Ujung-ujung batang bertemperatur 0 °C dan 20 °C. Banyaknya kalor yang merambat tiap sekon ialah ....
a. 0,1 kal/s
b. 0,2 kal/s
c. 0,5 kal/s
d. 0,7 kal/s
e. 10 kal/s
Kunci Jawaban :
Diketahui:
KAl = 500 × 10–1 kal/m s °C,
AAl = 1 cm2 = 10–4 m2, dan
ΔT = (20 – 0) = 20 °C.
Banyaknya kalor yang merambat tiap sekon :
(di sini L dianggap 1 m), jadi :
H = KA ΔT
H = (500)(10–1) (20) (10–4)
H = 0,1 kal/s
Contoh Soal 10 :
Batang logam dengan panjang 2 meter, mempunyai luas penampang 20 cm2 dan perbedaan temperatur kedua ujungnya 50 °C. Jika koefisien konduksi termalnya 0,2 kal/ms°C, tentukanlah jumlah kalor yang dirambatkan per satuan luas per satuan waktu.
Kunci Jawaban :
Diketahui:
K = 0,2 kal/ms °C,
L = 2 meter,
ΔT = 50 °C, dan
A = 20 cm2 = 2 × 10–3 m2.
Dengan memakai Persamaan (1–16), diperoleh :
H = 0,2 kal/ms°C × (2× 10–3 m2) × (50 °C / 2 m)
H = 0,01 kal/s
H = 0,01 kal/s
2. Perpindahan Kalor Secara Konveksi
Perambatan kalor yang disertai perpindahan massa atau perpindahan partikel- partikel zat perantaranya disebut perpindahan kalor secara fatwa atau konveksi. Rambatan kalor konveksi terjadi pada fluida atau zat alir, menyerupai pada zat cair, gas, atau udara.
 |
| Gambar 6. Rambatan kalor di dalam gas. |
Apabila dua sisi yang berhadapan dari silinder pada Gambar 6. suhunya berbeda, akan terjadi fatwa kalor dari dinding yang bersuhu Ta ke dinding yang bersuhu Tb. Besarnya kalor yang merambat tiap satuan waktu, sanggup dituliskan sebagai berikut.
H = hA ΔT (1-18)
dengan:
H = jumlah kalor yang berpindah tiap satuan waktu,
H = jumlah kalor yang berpindah tiap satuan waktu,
A = luas penampang aliran,
ΔT = perbedaan temperatur antara kedua daerah fluida mengalir, dan
h = koefisien konveksi termal.
Besarnya koefisien konveksi termal dari suatu fluida bergantung pada bentuk dan kedudukan geometrik permukaan-permukaan bidang fatwa serta bergantung pula pada sifat fluida perantaranya.
Contoh Soal 10 :
Suatu fluida dengan koefisien konveksi termal 0,01 kal/ms °C mempunyai luas penampang fatwa 20 cm2. Jika fluida tersebut mengalir dari dinding yang bersuhu 100 °C ke dinding lainnya yang bersuhu 20 °C, kedua dinding sejajar. Berapakah besarnya kalor yang dirambatkan?
Kunci Jawaban :
Diketahui:
h = 0,01 kal/ms °C,
Ta = 100 °C,
Tb = 20 °C, dan
A = 20 cm2 = 2 × 10–3 m2.
Dengan memakai Persamaan (1–18), diperoleh
H = hA ΔT
H = 0,01 kal/ms °C × (2 × 10–3 m2) × (100 °C – 20 °C) = 16 × 10–4 kal/s
Jadi, besarnya kalor yang merambat dalam fluida per satuan waktu ialah 16 × 10–4 kal/s.
Catatan Fisika :
Lemari es membantu hambar dengan fatwa arus konveksi. Udara hambar terdapat pada penggalan atas lemari es, sementara udara hangat yang terdapat pada penggalan bawah bergerak naik, kemudian menjadi lebih dingin.
3. Perpindahan Kalor Secara Radiasi
Matahari merupakan sumber energi utama bagi insan di permukaan bumi ini. Energi yang dipancarkan Matahari hingga di Bumi berupa gelombang elektromagnetik. Cara perambatannya disebut sebagai radiasi, yang tidak memerlukan adanya medium zat perantara. Semua benda setiap ketika memancarkan energi radiasi dan kalau telah mencapai kesetimbangan termal atau temperatur benda sama dengan temperatur lingkungan, benda tersebut tidak akan memancarkan radiasi lagi. Dalam kesetimbangan ini, jumlah energi yang dipancarkan sama dengan jumlah energi yang diserap oleh benda tersebut.
Dari hasil percobaan yang dilakukan oleh Josef Stefan dan Ludwig Boltzmann, diperoleh besarnya energi per satuan luas per satuan waktu yang dipancarkan oleh benda yang bersuhu T, yakni
W = eσ T4 (1–19)
dengan:
W = energi yang dipancarkan per satuan luas per satuan waktu (watt/m2),
σ = konstanta Stefan–Boltzmann = 5,672 × 10–8 watt/m2 K4,
T = temperatur mutlak benda (K), dan
e = koefisien emisivitas (0 < e ≤ 1).
Percobaan Fisika Sederhana 2 :
Catatlah temperatur air panas yang berada di dalam sebuah wadah dengan memakai termometer. Kemudian, masukkan air hambar ke dalam wadah tersebut dan catat temperatur simpulan campuran. Sebelumnya, catat massa air panas, air dingin, dan temperatur awal air dingin, kemudian tuliskan data hasil pengamatan Anda dalam bentuk tabel. Apa yang sanggup Anda simpulkan? Laporkan hasil pengamatan kepada guru Anda dan persentasikan di depan kelas.
Contoh Soal 11 :
Suatu kalorimeter berisi es (kalor jenis es = 0,5 kal/gK, kalor lebur es = 80 kal/g) sebanyak 36 g pada temperatur – 6 °C. Kapasitas kalorimeter ialah 27 kal/K. Kemudian, ke dalam kalorimeter tersebut dituangkan alkohol (kalor jenis 0,58 kal/gK) pada temperatur 50° yang menyebabkan temperatur simpulan menjadi 8 °C. Massa alkohol yang dituangkan (dalam gram) ialah ....
a. 108
b. 150
c. 200
d. 288
e. 300
Kunci Jawaban :
Diketahui:
Tes = –6 °C,
Tes = –6 °C,
C = 27 kal/K,
mes = 36 g,
ces = 0,5 kal/gK,
Les = 80 kal/g,
cair = 1 kal/gK,
Talkohol = 50°C,
cal = 0,58 kal/gK, dan
temperatur simpulan T = 8 °C.
Berlaku Asas Black yang menyatakan kalor yang diserap sama dengan kalor yang dilepaskan. Es menyerap kalor, suhunya naik menjadi 0°C, kemudian melebur menjadi air, kemudian naik suhunya menjadi 8 °C. Kalor yang diserap es ialah :
Qes = mes ces ΔT + mes Les + mes ces ΔT
Qes = 36 × 0,5 × (0 – (–6)) + 36 × 80 + 36 × 1 × 8
Qes = 3.276 kalori
Pada kalorimeter, temperatur naik dari –6 °C menjadi 8 °C sehingga kalorimeter menyerap panas sebesar :
Qkal = C ΔT
Qkal = 27 × (8 – (–6))
Qkal= 378 kalori
Kalor yang dilepas alkohol diserap oleh es dan kalori meter sehingga
Qkal = Qes + Qkal
malkohol calkohol ΔT = 3.276 + 378
malkohol × 0,58 × 42 = 3.654
malkohol = 150 gram
Jadi, massa alkohol yang harus dituangkan supaya temperatur simpulan menjadi 8 °C ialah sebesar 150 gram.
Jawab: d
Rangkuman :
1. Sifat fisik suatu benda untuk memilih apakah telah terjadi kesetimbangan termal disebut dengan temperatur atau temperatur dan sanggup diukur dengan alat yang disebut termometer.
2. Ketika mengukur temperatur dengan memakai termometer, terdapat beberapa skala yang digunakan, di antaranya skala Celsius, skala Reamur, skala Fahrenheit, dan skala Kelvin.
3. Jika suatu zat dipanaskan, akan mengalami pemuaian panjang, pemuaian luas, dan pemuaian volume.
4. Kalor didefinisikan sebagai perpindahan energi dari suatu zat ke zat lainnya dengan diikuti perubahan temperatur.
5. Kalor jenis suatu benda didefinisikan sebagai jumlah kalor yang diharapkan untuk menaikkan temperatur 1 kg suatu zat sebesar 1 K.
6. Besarnya kalor suatu benda sanggup dituliskan ke dalam persamaan :
Q = mc Δt
7. Suatu zat sanggup berkembang menjadi tiga wujud zat, di antaranya cair, padat, dan gas. Perubahan wujud zat ini diikuti dengan perembesan dan pelepasan kalor.
8. Kalor penguapan ialah kalor yang dibutuhkan oleh suatu zat untuk menguapkan zat tersebut.
9. Secara matematis, besarnya kalor peleburan, penguapan, pembekuan, dan penyubliman adalah
Q = mL
10. Asas Black menyampaikan bahwa energi ialah awet sehingga benda yang mempunyai temperatur lebih tinggi akan melepaskan energi sebesar QL dan benda yang mempunyai temperatur lebih rendah akan mendapatkan energi sebesar QT dengan besar yang sama.
11. Kalor sanggup merambat dengan tiga cara, di antaranya secara konduksi (hantaran), secara konveksi (aliran), dan secara radiasi (pancaran).
Anda kini sudah mengetahui Temperatur, Perpindahan Kalor, dan Pemuaian Zat. Terima kasih anda sudah berkunjung ke Perpustakaan Cyber.
Referensi :
Saripudin, A., D. Rustiawan K., dan A. Suganda. 2009. Mudah Belajar Fisika 1 : untuk Kelas 10 Sekolah Menengah Atas / Madrasah Aliyah Program Ilmu Pengetahuan Alam. Pusat Perbukuan Departemen Nasional, Departemen Pendidikan Nasional, Jakarta. 194 hlm.